Sinds de invoering van de European Clinical Trial Regulation (CTR) in januari 2022 werken we in Nederland hard aan een efficiëntere en geharmoniseerde opstart van klinisch onderzoek.
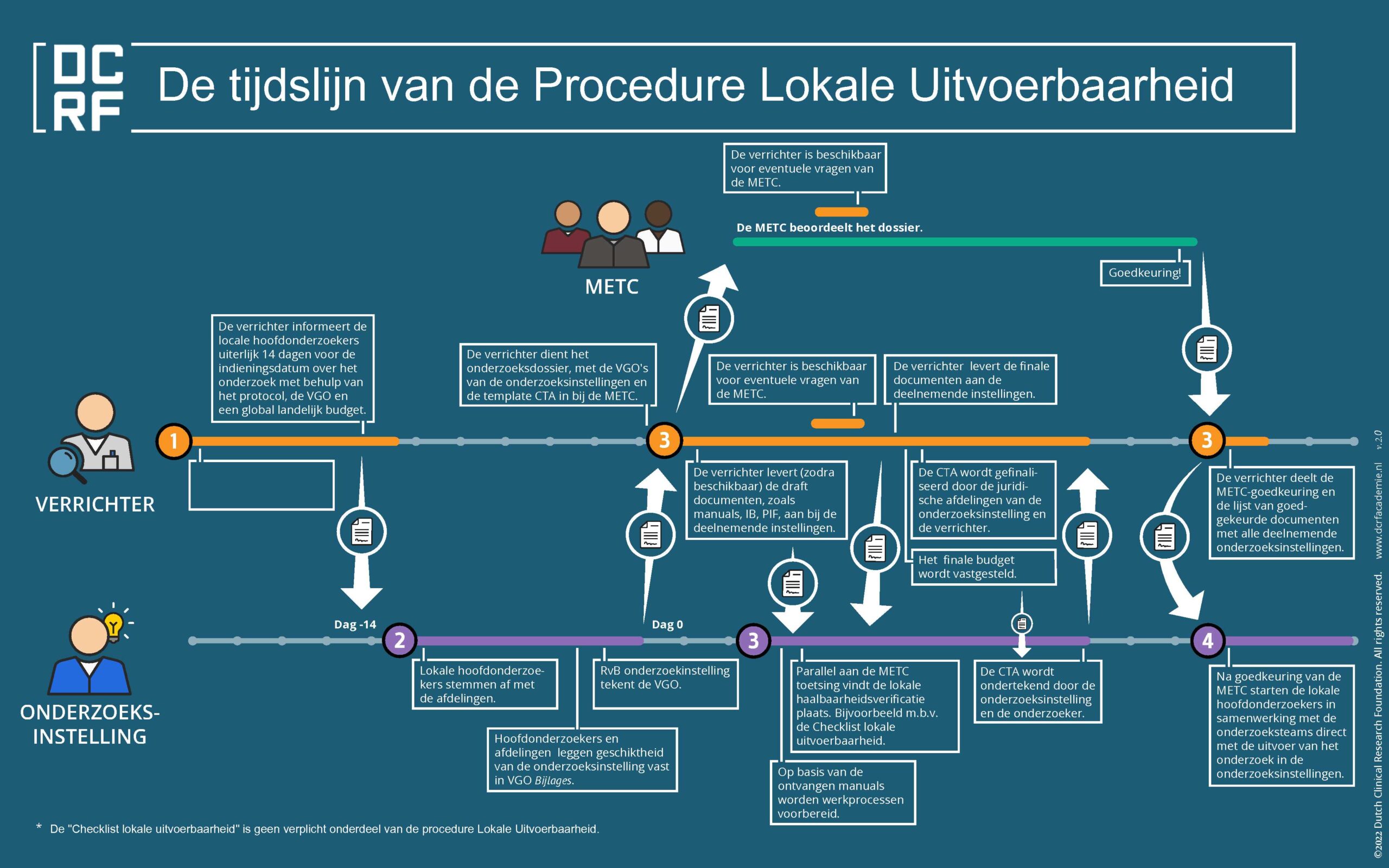
Een belangrijke stap hierin is de Procedure Lokale Uitvoerbaarheid, ontwikkeld binnen de DCRF. Deze procedure zorgt ervoor dat alle betrokken partijen – van verrichter tot Raad van Bestuur – parallel toewerken naar hetzelfde doel: een snelle, zorgvuldige en goed afgestemde opstart van geneesmiddelenonderzoek direct na centrale goedkeuring.
Waarom is parallel werken zo belangrijk?
Door de processen in de deelnemende ziekenhuizen parallel te laten lopen met de Europese toetsing kan onderzoek direct na goedkeuring in heel Europa van start. Sneller starten betekent uiteindelijk dat innovatie sneller de patiënt bereikt.
Belangrijke onderdelen van dit traject zijn:
VGO – Kan de instelling het onderzoek uitvoeren?
CTA – Gaat de instelling het onderzoek uitvoeren?
CTIS-autorisatie – Mag de instelling het onderzoek uitvoeren?
Door deze processen parallel te laten verlopen, minimaliseren we vertraging en vergroten we de impact van klinisch onderzoek in Nederland.
Meer weten over de procedure, downloads of tools nodig? Bezoek: Procedure Lokale Uitvoerbaarheid – Dutch Clinical Research Foundation
Samen versnellen we innovatie in de zorg.